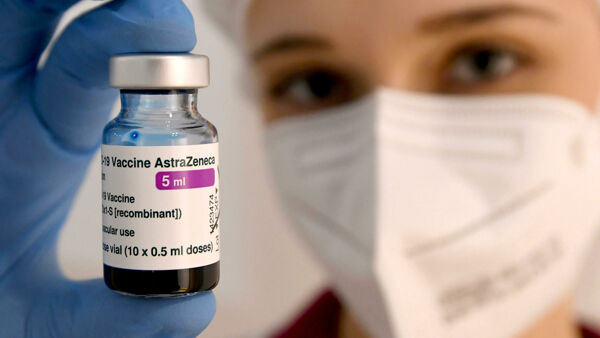
L'Agenzia italiana del farmaco (Aifa) “approva la vaccinazione mista per i soggetti under 60 che abbiano ricevuto una prima dose di vaxzevria” (AstraZeneca). E' quanto si legge nel parere di Aifa appena pubblicato ieri sera. “Sulla base di studi clinici pubblicati nelle ultime settimane, la Commissione tecnico scientifica – si legge – ha ritenuto, a fronte di un rilevante potenziamento della risposta anticorpale e un buon profilo di reattogenicità, di approvare il mix vaccinale (prima dose con Vaxzevria e seconda dose con Comirnaty – Pfizer, per analogia, con il vaccino Moderna)”.
L'AIFA ha, dunque, espresso parere favorevole all'utilizzo dei dei vaccini a mRNA per somministrare la seconda dose e completare un ciclo vaccinale misto ai soggetti di età inferiore ai 60 anni che abbiano già effettuato una prima dose di vaccino Vaxzevria (Astrazeneca)”. Il Comitato Tecnico Scientifico ha ritenuto che la seconda somministrazione con vaccino a mRNA possa avvenire a distanza di 8-12 settimane dalla somministrazione di Vaxzevria. Quanto all'EMA (l'Agenzia europea dei Medicinali), la posizione su AstraZeneca non cambia: "Il bilancio rischi-benefici resta positivo – fanno sapere attraverso una nota – e il vaccino resta autorizzato per tutta la popolazione". Per l'EMA rimangono validi tutti i quattro vaccini anti-Covid approvati in Europa. E' corso, poi, lo studio clinico del vaccino dell'azienda Curevac, con sede in Germania, che potrebbe arrivare all'esame dell'Ema verso fine estate: per l'Europa potrebbe diventare il quinto vaccino anti Covid e il terzo a mRna.